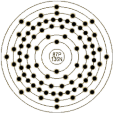
钫是门捷列夫曾经指出的类铯,是莫斯莱所确定的原子序数为87的元素。它的发现经历了弯曲的道路。
刚开始,化学家们根据门捷列夫的推断――类铯是一个碱金属元素,是成盐的元素,就尝试从各种盐类里去寻找它,但是一无所获。|
元素 名称 |
|
元素符号 |
|
原子 序数 |
|
相对原子质量 (12C = 12.0000) |
|
||||
| 英文名称 |
|
|
原 子 结 构 |
|
|
发 现 |
|
|
来 源 |
|
|
物 理 性 质 |
|
||||||||||||||||
|
化 学 性 质 |
|
|||||||
|
地 质 数 据 |
|
|
生 物 数 据 |
|